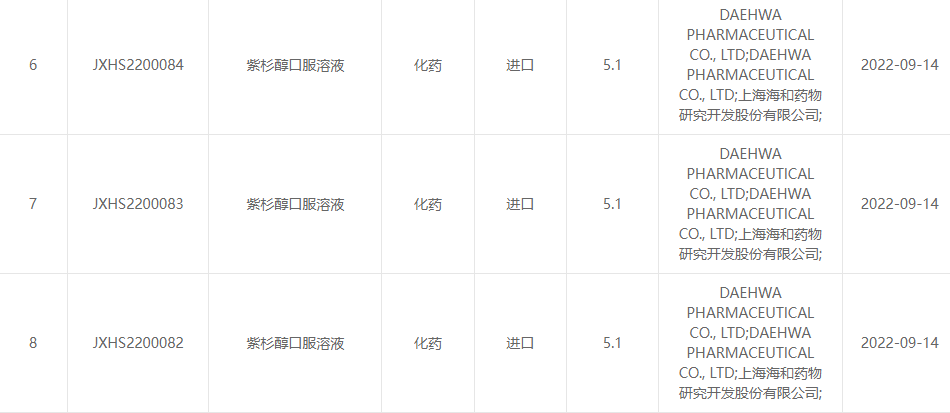
13 вересня 2022 року Shanghai Haihe Pharmaceutical Research and Development Co., Ltd. і Daehwa Pharmaceutical Co., Ltd. спільно оголосили, що пероральний розчин паклітакселу (RMX3001), спільно розроблений двома сторонами, був офіційно схвалений Центром лікарських засобів. Оцінка (CDE) Держлікслужби.(Номер прийняття: країна JXHS2200082, країна JXHS2200083, країна JXHS2200084).
Джерело фото: Держлікслужба
Паклітакселшироко використовується при лікуванні різних злоякісних пухлин, таких як рак легенів, рак молочної залози, рак яєчників, рак голови та шиї та рак шлунка.Полімеризація білка, складання мікротрубочок, запобігання деполімеризації, тим самим стабілізація мікротрубочок і інгібування мітозу ракових клітин і запуск апоптозу, тим самим ефективно запобігаючи проліферації ракових клітин і відіграючи протиракову дію.
На даний момент у більшості країн світу використовується паклітаксел у формі ін’єкцій, які потрібно розробляти та вводити внутрішньовенно крапельно в лікарні.Пацієнти повинні часто повертатися до лікарні, і в місці ін’єкції будуть побічні реакції.Тому розробка пероральних препаратів паклітакселу завжди була гарячою точкою в галузевих дослідженнях..
RMX3001 — пероральна композиція паклітакселу, розроблена компанією Dahua Pharmaceutical на основі її інноваційної технології доставки ліків, що самоемульгують ліпіди.У вересні 2016 року його схвалило Управління з контролю за продуктами й ліками Кореї (торгова назва Liporaxel), і показанням є розширена терапія або терапія другої лінії метастатичного раку шлунка або місцевого рецидиву раку шлунка.Відповідно до прес-релізу Haihe Pharmaceuticals, Liporaxel є першим пероральним препаратом паклітакселу, який на сьогоднішній день успішно розроблено та схвалено для продажу у світі.У вересні 2017 року Haihe Pharmaceutical отримала від Dahua Pharmaceuticals права на дослідження та розробки, виробництво та продаж продукту в Китаї, Гонконзі, Тайвані та Таїланді.
Заявка на реєстрацію RMX3001 у Китаї в основному ґрунтується на рандомізованих, відкритих, паралельно контрольованих, багатоцентрових клінічних дослідженнях 3 фази не меншої ефективності, які мають на меті порівняти другу лінію лікування пероральним розчином паклітакселу RMX3001 та паклітаксел для ін’єкцій (таксол) Ефективність і безпека у пацієнтів із прогресуючим раком шлунка.Дослідження спільно проводили професор Лі Цзінь з Шанхайської східної лікарні та професор Цінь Шукуй з лікарні Нанкін Цзіньлінг як головні дослідники.
Доктор Руйпінг Донг, головний виконавчий директор Haihe Pharmaceuticals, сказав: «Прийняття заявки на пероральний розчин паклітакселу (RMX3001) є ще однією важливою віхою для Haihe Pharmaceuticals, і я дуже вдячний клінічним дослідникам і пацієнтам, які брали участь у нашому суд.Поширений рак шлунка. Досі існує величезна незадоволена клінічна потреба в лікуванні, і ми сподіваємося якнайшвидше запропонувати найсучасніші інноваційні та зручні методи лікування пацієнтам у Китаї та в усьому світі».
Yunnan Hande Biotechnology Co., Ltd. протягом 28 років займається виробництвом паклітакселу.Це перший у світі незалежний виробник рослинного протипухлинного препарату паклітаксел, який був схвалений FDA США, Європейським EDQM, Австралійським TGA, Китаєм CFDA, Індією, Японією та іншими національними регуляторними органами.підприємства.Якщо ви хочете купитиПаклітаксел API,будь ласка, зв'яжіться з нами онлайн.
Час публікації: 14 вересня 2022 р